近日,由新葡萄8883官网AMG常超教授团队与复旦大学舒友生课题组、上海理工大学宋波课题组、中国科学技术大学温泉课题组、中科院化学所毛兰群课题组合作,在神经调控机制方面的研究取得重大突破。该研究发现中红外光刺激(Midinfrared Stimulation,MIRS)能够作为一种新型的神经调控(Neuromodulation)策略,调节神经元的信号发生、动作电位波形,以及动物行为,并且这种调控作用具有非热、可逆、长距离的特点。
红外神经刺激(Infrared neural stimulation)是神经调控策略之一,目前主要是将近红外光(1.2-2.2微米)直接作用于神经组织,从而激活或抑制神经元上动作电位的发放,进而调节脑的功能。红外神经刺激的作用机理被普遍认为是光热作用,即红外光被水吸收而产热,温度的突然变化在细胞上产生跨膜电容电流或激活了热敏感离子通道,进而影响神经细胞的电活动。但是,过量的光热作用往往会引起细胞和组织的损伤。为了避免红外的热效应,该工作的研究团队将目光投向中红外光(2.5-25微米波长),特别是水吸收较低的中红外波长(如3.5-5.7微米,相应频率为85.6-52.6 THz)。由于动作电位的产生依赖于细胞膜上离子通道蛋白的活动(包括通道的开放、关闭、离子筛选和通透等),特别是电压门控钠通道和钾通道,而这些生物大分子内部化学键的振动频率处于中红外区间。如果特定频率的中红外光与离子通道的关键化学键形成共振则可能调控通道的功能,从而影响神经元的电活动。

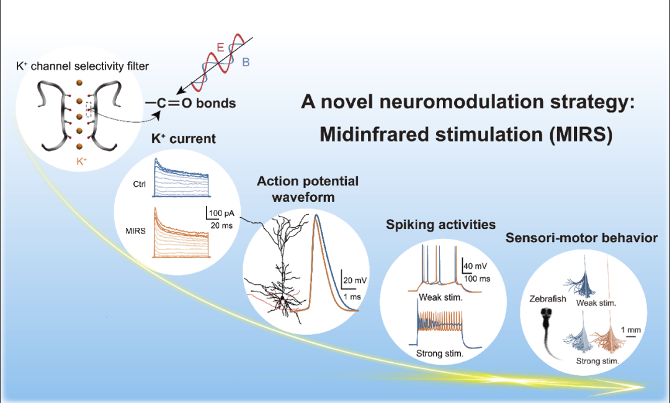
基于上述思路,该研究结合电生理、分子模拟、光场成像等不同领域的前沿技术,在分子、细胞、整体行为三个层面进行了系统的研究,发现5.6微米波长的中红外刺激(MIRS)能够以非热的方式调控神经信号和行为。在分子水平,发现钾通道内负责钾离子选择性的功能域上富集的羰基(-C=O),共振吸收了MIRS的光子能量,导致钾离子的通透性提高、钾电流增加;实验同时观察到MIRS的效应随着光纤尖端与神经元之间的距离(d)增加而缓慢衰减,呈现1/d衰减规律,而不是1/d2。这种反常现象提示神经元可能存在一种对中红外光子的量子捕获效应(Quantum-harvesting effect)。在细胞水平,增加的钾电流一方面使得神经元的输出信号—动作电位的波形变得狭窄,另一方面产生了分流效应(Shunting effect),从而使细胞对弱刺激响应更弱,对强刺激的反应更强,表现出增益调控(Gain modulation)。在整体动物行为水平,MIRS调控了斑马鱼由不同强度刺激引起的逃跑行为,即在MIRS作用下,动物行为对刺激“遇弱则弱,遇强更强”。因此,MIRS可以作为一种新型的神经调控手段,以无创、非热、可逆的方式调节神经活动和行为,具有潜在脑功能调控和脑疾病治疗的临床应用价值。
该研究相关成果2021年3月1日以“Nonthermal and reversible control of neuronal signaling and behavior by midinfrared stimulation”为题在《美国科学院院报》(PNAS,IF = 9.41)在线发表。新葡萄8883官网AMG博士生乔智为论文共同第一作者(排名第二)。常超教授为共同通讯作者。该研究得到了国家自然科学基金项目(31630029,31661143037,11622542以及31430038)、创新特区项目、国家重点研发计划项目(2018YFE0205501)的资助。
论文网址:
https://doi.org/10.1073/pnas.2015685118
(PNAS, 118 (10): e2015685118)

